De har modtaget en advarselsbrev.
Hverdagen byder på mange små beslutninger om sundhed.
Flere danskere holder øje med nye behandlinger og medicin, som kan gøre livet lettere.
Apoteket og lægens råd fylder derfor mere i mange familiers samtaler.
Samtidig følger både patienter og myndigheder nøje med i, hvordan medicin bliver testet og kontrolleret.
Sikkerhed omkring lægemidler er nemlig afgørende for tilliden til hele sundhedssystemet.
Derfor vækker nye meldinger fra internationale sundhedsmyndigheder ofte stor opmærksomhed.
Det skriver EkstraBladet.
Hvad sagen handler om
Novo Nordisk står nu midt i en sag hos den amerikanske fødevare og lægemiddelmyndighed FDA.
Ifølge det amerikanske medie CBS News har myndigheden sendt et advarselsbrev til selskabet.
Brevet er dateret 5. marts og handler om, hvordan mulige bivirkninger er blevet indrapporteret til myndighederne.
FDA henviser blandt andet til tre dødsfald blandt patienter, som har fået behandling med medicin, der indeholder stoffet semaglutid.
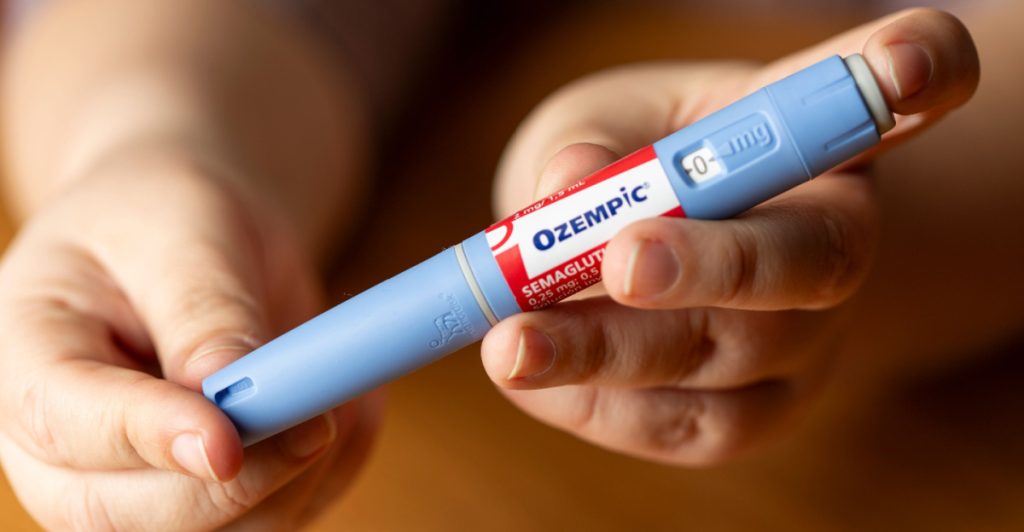
Semaglutid er det aktive stof i diabetesmidlet Ozempic og vægttabsmidlet Wegovy, som også er kendt blandt mange danskere.
Ifølge FDA indgår der i materialet et selvmord blandt de tre dødsfald. Der er også omtale af en patient med selvmordstanker.
Myndigheden konkluderer ikke, at medicinen er årsag til dødsfaldene eller andre reaktioner.
Fokus i brevet handler i stedet om, hvorvidt regler for indrapportering af mulige bivirkninger er blevet fulgt korrekt.
CBS News skriver, at kontrollører fra FDA opdagede problemer under et tilsyn i begyndelsen af 2025.
Besøget fandt sted på Novo Nordisks amerikanske hovedkontor i Plainsboro i New Jersey.
Reaktion fra Novo
Novo Nordisk bekræfter i en pressemeddelelse, at selskabet modtog brevet 5. marts 2026. Her fremgår det også, at sagen udspringer af en inspektion 7. februar 2025.
Virksomheden oplyser, at der siden besøget er arbejdet målrettet på at håndtere myndighedens observationer.
Ifølge selskabet har FDA løbende fået orientering om arbejdet. Det er sket gennem syv tilbagemeldinger til myndigheden.
Anna Windle, der er direktør for klinisk udvikling i Novo Nordisk i USA, forventer en løsning på sagen.
“Vi er sikre på, at vi vil løse de forhold, der er beskrevet i advarselsbrevet, til FDA’s fulde tilfredshed,” skriver Anna Windle i en pressemeddelelse fra Novo Nordisk.
Sagen bliver nu fulgt tæt, også fra dansk side, hvor Novo Nordisk fylder meget i både økonomien og sundhedsdebatten.